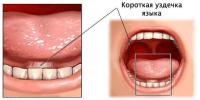
Состав и строение фенола. Получение, химические свойства и применение фенола
На рисунке показана взаимосвязь различных методов производства фенола, а в таблице под теми же номерами приведены их технико-экономические показатели (в % относительно сульфонатного метода).
Рис. 1.1. Методы производства фенола
Таблица 1.3
Технико-экономические показатели производства фенола| Методы | ||||||
| Показатель | 1 | 2 | 3 | 4 | 5 | 6 |
| Капитальные затраты | 100 | 83 | 240 | 202 | 208 | 202 |
| Стоимость сырья | 100 | 105 | 58 | 69 | 72 | 45 |
| Себестоимость | 100 | 96 | 70 | 73 | 76 | 56 |
Таким образом, наиболее целесообразным с экономической точки зрения является наиболее востребованный в настоящее время кумольный процесс. Ниже кратко описаны промышленные процессы, которые в то или иное время использовались для получения фенола.
1. Сульфонатный процесс был первым фенольным процессом, реализованным в промышленном масштабе фирмой «BASF» в 1899 г. Этот метод основан на сульфировании бензола серной кислотой с последующим щелочным плавлением сульфокислоты. Несмотря на применение агрессивных реагентов и образование большого количества отходов сульфита натрия, данный метод использовался в течение почти 80 лет. В США это производство было закрыто лишь в 1978 году.
2. В 1924 г. фирмой «Dow Chemical» был разработан процесс получения фенола, включающий реакцию хлорирования бензола и последующий гидролиз монохлорбензола (процесс каталитического гидролиза галогензамещенных бензолов ). Независимо аналогичная технология была разработана немецкой фирмой «I.G. Farbenindustrie Co». Впоследствии стадия получения монохлорбензола и стадия его гидролиза были усовершенствованы, и процесс получил название «процесс Рашига». Суммарный выход фенола по двум стадиям составляет 70-85%. Данный процесс был основным методом получения фенола в течение нескольких десятилетий.
3. Циклогексановый процесс , разработанный фирмой «Scientific Design Co.», основан на окислении циклогексана в смесь циклогексанона и циклогексанола, которая далее дегидрируется с образованием фенола. В 60-е годы фирма «Monsanto» в течение нескольких лет использовала этот метод на одном из своих заводов в Австралии, однако в дальнейшем перевела его на кумольный способ получения фенола.
4. В 1961 г. фирмой «Dow Chemical of Canada» был реализован процесс через разложение бензойной кислоты , это единственный способ синтеза фенола, основанный на использовании небензольного сырья. Обе реакции протекают в жидкой фазе. Первая реакция. окисление толуола. использовалась в Германии уже в период Второй мировой войны для получения бензойной кислоты. Реакция протекает в довольно мягких условиях с высоким выходом. Вторая стадия является более трудной вследствие дезактивации катализатора и низкой селективности по фенолу. Полагают, что проведение этой стадии в газовой фазе может сделать процесс более эффективным. В настоящее время этот метод используется на практике, хотя его доля в мировом производстве фенола составляет лишь около 5%.
5. Метод синтеза, по которому в наши дни получают большую часть производимого в мире фенола - кумольный процесс - открыт группой советских химиков во главе с профессором П. Г. Сергеевым в 1942 году. Метод основан на окислении ароматического углеводорода кумола (изопропилбензол) кислородом воздуха с последующим разложением получающейся гидроперекиси, разбавленной серной кислотой. В 1949 году в г. Дзержинске Горьковской области был введен в действие первый в мире кумольный завод. До этого гидроперекиси считались малостабильными промежуточными продуктами окисления углеводородов. Даже в лабораторной практике их почти не использовали. На Западе кумольный метод был разработан в конце 40-х годов и отчасти известен как процесс Хока, по имени немецкого ученого, позднее независимо открывшего кумольный путь синтеза фенола. В ромышленном масштабе этот метод стал впервые использоваться в США в начале 50-х годов. С этого времени на многие десятилетия кумольный процесс становится образцом химических технологий во всем мире.
Несмотря на прекрасно отлаженную технологию и длительный опыт эксплуатации, кумольный метод имеет ряд недостатков. Прежде всего это наличие взрывоопасного промежуточного соединения (гидропероксид кумола), а также многостадийность метода, что требует повышенных капитальных затрат и делает труднодостижимым высокий выход фенола в расчете на исходный бензол. Так, при выходе полезного продукта 95% на каждой из трех стадий итоговый выход составит лишь 86%. Приблизительно такой выход фенола и дает кумольный метод в настоящее время. Но самый важный и принципиально неустранимый недостаток кумольного метода связан с тем, что в качестве побочного продукта образуется ацетон. Это обстоятельство, которое первоначально рассматривалось как сильная сторона метода, становится все более серьезной проблемой, поскольку ацетон не находит эквивалентного рынка сбыта. В 90-х годах эта проблема стала особенно ощутимой после создания новых способов синтеза метилметакрилата путем окисления углеводородов С4, что резко сократило потребность в ацетоне. Об остроте ситуации говорит тот факт, что в Японии разработана технология, предусматривающая рецикл ацетона. С этой целью к традиционной кумольной схеме добавляются еще две стадии, гидрирование ацетона в изопропиловый спирт и дегидратация последнего в пропилен. Образующийся пропилен снова возвращают на стадию алкилирования бензола. В 1992 году фирма «Mitsui» пустила крупное производство фенола (200 тыс. т/год), основанное на этой пятистадийной кумольной технологии.

Рис. 1.2. Рецикл ацетона с получением пропилена
Предлагаются также другие сходные модификации кумольного метода, которые позволили бы смягчить проблему ацетона. Однако все они приводят к значительному усложнению технологии и не могут рассматриваться как перспективное решение проблемы. Поэтому исследования, ориентированные на поиск новых путей синтеза фенола, которые основывались бы на прямом окислении бензола, в последнее десятилетие приобрели особенно интенсивный характер. Работы ведутся главным образом в следующих направлениях: окисление молекулярным кислородом, окисление моноатомными донорами кислорода и сопряженное окисление. Рассмотрим более подробно направления поиска новых путей синтеза фенола.
Основная цель этого процесса состоит в производстве металлургического кокса. Побочно образуются жидкие продукты коксования и газ. Перегонкой жидких продуктов коксования наряду с бензолом, толуолом и нафталином получают фенол, тиофен, пиридин и их гомологи, а также более сложные аналоги с конденсированными ядрами. Доля каменноугольного фенола,по сравнению с получаемым кумольным методом, незначительна.
2. Замещение галогена в ароматических соединениях
Замещение галогена на гидроксильную группу протекает в жестких условиях и известно как «Дау»-процесс (1928 г.)
Раньше этим способом получали фенол (из хлорбензола), но теперь его значение снизилось в связи с разработкой более экономичных способов, не связанных с затратами хлора и щелочи и образованием большого количества сточных вод.
В активированных галогенаренах (содержащих наряду с галогеном нитрогруппу в о- и п- положениях) замещение галогена протекает в более мягких условиях:

Это можно объяснить электроноакцепторным влиянием нитрогруппы, которая оттягивает на себя электронную плотность бензольного кольца и таким образом участвует в стабилизации σ-комплекса:

3. Способ Рашига
Это видоизмененный хлорный метод: бензол подвергается окислительному хлорированию действием хлористого водорода и воздуха, и затем, не выделяя образовавшийся хлорбензол, гидролизуют его водяным паром в присутствии солей меди. В результате хлор вообще не расходуется, а суммарный процесс сводится к окислению бензола в фенол:
4.Сульфонатный способ
Фенолы можно получить с хорошим выходом при сплавлении ароматических сульфокислот Ar-SO 3 H со смесью гидроксидов натрия и калия (реакция щелочного плавления ) при 300С с последующей нейтрализацией образующегося алкоголята путем добавления кислоты:

Метод эксплуатируется в промышленности до сих пор (для получения фенола) и используется в лабораторной практике.
5. Кумольный метод
Первое крупное производство фенола кумольным методом было осуществлено в 1949 г. в Советском Союзе. В настоящее время это основной метод получения фенола и ацетона.
Метод включает две стадии: окисление изопропилбензола (кумола) кислородом воздуха до гидропероксида и его кислотное разложение:

Преимуществом данного метода является отсутствие побочных продуктов и высокая потребность конечных продуктов – фенола и ацетона. Метод был разработан в нашей стране Р.Ю. Удрисом, Б.Д. Круталовым и др. в 1949 г.
6. Из солей диазония
Метод заключается в нагревании солей диазония в разбавленной серной кислоте, что приводит к гидролизу – замене диазогруппы на гидроксигруппу. Синтез весьма удобен для получения гидроксиаренов в лабораторных условиях:

Строение фенолов
Строение и распределение электронной плотности в молекуле фенола можно изобразить следующей схемой:

Дипольный момент фенола составляет 1.55 Д и направлен в сторону бензольного кольца. Гидроксильная группа по отношению к бензольному кольцу проявляет –I эффект и +М эффект. Так как мезомерный эффект гидроксигруппы преобладает над индукционным, сопряжение неподеленных электронных пар атома кислорода с -орбиталями бензольного кольца оказывает электронодонорное влияние на ароматическую систему, что повышает ее реакционную способность в реакциях электрофильного замещения.
Фенол представляет собой бесцветное вещество кристаллического строения с весьма специфическим запахом. Данная субстанция достаточно широко используется в производстве различных красителей, пластмасс, разнообразных синтетических волокон (в основном капрона). До развития нефтехимической отрасли получение фенола осуществлялось исключительно из каменноугольных смол. Конечно же, этот способ был не в состоянии покрыть все потребности бурно развивающейся промышленности в феноле, который сейчас стал важным компонентом едва ли не всех окружающих нас предметов.
Фенол, получение которого стало насущной необходимостью в связи с появлением чрезвычайно широкого спектра новых материалов и веществ, неотъемлемым ингредиентом которых он является, используется в процессе синтеза А она, в свою очередь, является важным компонентом фенопластов. Также большое количество фенола перерабатывается в циклогексанол, необходимый для изготовления в промышленных масштабах.

Еще из важных сфер можно выделить производство смеси креозолов, которую синтезируют в креозолформадельгидную смолу, используемую для изготовления множества медицинских препаратов, антисептиков и антиоксидантов. Поэтому сегодня получение фенола в больших количествах является важной задачей нефтехимии. Уже разработано немало методов, позволяющих производить это вещество в достаточных объемах. Остановимся на основных из них.
Наиболее старым и проверенным методом является способ щелочного плавления, который характеризуется большим расходом серной кислоты для и каустика с последующим сплавлением их в бензолсульфонатриевую соль, из которой непосредственно и выделяется данное вещество. Получение фенола методом хлорирования бензола с последующим омылением хлорбензола рентабельно только в случае наличия большого количества дешевой электроэнергии, необходимой для производства каустика и хлора. Главные недостатки данной методики - необходимость создания высокого давления (не менее трехсот атмосфер) и чрезвычайно значительная степень коррозии аппаратуры.

Более современным методом является получение фенола путем разложения гидроперекиси изопропилбензола. Правда, схема выделения требуемого вещества здесь довольно сложна, поскольку предусматривает предварительное производство гидроперекиси способом алкилирования бензола раствором пропилена. Далее технологией предусматривается окисление получившегося изопропилбензола воздушной смесью до образования гидроперекиси. В качестве положительного фактора данной методики можно отметить получение параллельно с фенолом еще одного важного вещества - ацетона.
Существует также методика выделения фенола из коксовых и полукоксовых смол твердых топливных материалов. Такая процедура необходима не только для получения ценного фенола, но также для повышения качества различных углеводородных продуктов. Одним из свойств фенола является быстрая окисляемость, что приводит к ускоренному старению масла и к образованию в нем вязких смолоподобных фракций.
Но самым современным методом и новейшим достижением нефтехимической отрасли является получение фенола из бензола напрямую путем окисления его Весь процесс производится в специальном адиабатическом реакторе, в котором находится цеолитсодержащий катализатор. Исходную закись азота получают окислением аммиака воздухом или выделением из Точнее, из ее побочных продуктов, образовывающихся в процессе синтеза. Данная технология способна обеспечить получение высокочистого фенола с минимальным суммарным содержанием примесей.
Образованные на основе бензола. При нормальных условиях представляют собой твердые ядовитые вещества, обладающие специфическим ароматом. В современной промышленности эти химические соединения играют далеко не последнюю роль. По объемам использования фенол и его производные входят в двадцатку наиболее востребованных химических соединений в мире. Они широко применяются в химической и легкой промышленности, фармацевтике и энергетике. Поэтому получение фенола в промышленных масштабах - одна из основных задач химической промышленности.
Обозначения фенола
Первоначальное название фенола - карболовая кислота. Позднее данное соединение поучило название «фенол». Формула этого вещества представлена на рисунке:
Нумерация атомов фенола ведется от того атома углерода, который соединен с гидроксогруппой ОН. Последовательность продолжается в таком порядке, чтобы другие замещенные атомы получили наименьшие номера. Производные фенола существуют в виде трех элементов, характеристики которых объясняются различием их структурных изомеров. Различные орто-, мета-, паракрезолы являются лишь видоизменением основной структуры соединения бензольного кольца и гидроксильной группы, базовая комбинация которой и представляет собой фенол. Формула этого вещества в химической записи выглядит как C 6 H 5 OH.
Физические свойства фенола
Визуально фенол представляет собой твердые бесцветные кристаллы. На открытом воздухе они окисляются, придавая веществу характерный розовый оттенок. При нормальных условиях фенол довольно плохо растворяется в воде, но с повышением температуры до 70 о этот показатель резко возрастает. В щелочных растворах это вещество растворимо в любых количествах и при любых температурах.

Эти свойства сохраняются и в других соединениях, основным компонентом которых являются фенолы.
Химические свойства
Уникальные свойства фенола объясняются его внутренней структурой. В молекуле этого химического вещества р-орбиталь кислорода образует единую п-систему с бензольным кольцом. Такое плотное взаимодействие повышает электронную плотность ароматического кольца и понижает этот показатель у атома кислорода. При этом полярность связей гидроксогруппы значительно увеличивается, и водород, входящий в ее состав, легко замещается любым щелочным металлом. Так образуются различные феноляты. Эти соединения не разлагаются водой, как алкоголяты, но их растворы очень похожи на соли сильных оснований и слабых кислот, поэтому они имеют достаточно выраженную щелочную реакцию. Феноляты взаимодействуют с различными кислотами, в результате реакции восстанавливаются фенолы. Химические свойства этого соединения позволяют ему взаимодействовать с кислотами, образуя при этом сложные эфиры. Например, взаимодействие фенола и уксусной кислоты приводит к образованию финилового эфира (фениацетата).

Широко известна реакция нитрирования, в которой под воздействием 20% азотной кислоты фенол образует смесь пара- и ортонитрофенолов. Если воздействовать на фенол концентрированной азотной кислотой, то получается 2,4,6-тринитрофенол, который иногда называют пикриновой кислотой.

Фенол в природе
Как самостоятельное вещество фенол в природе содержится в каменноугольной смоле и в отдельных сортах нефти. Но для промышленных нужд это количество не играет никакой роли. Поэтому получение фенола искусственным способом стало приоритетной задачей для многих поколений ученых. К счастью, эту проблему удалось разрешить и получить в итоге искусственный фенол.
Свойства, получение
Применение различных галогенов позволяет получать феноляты, из которых при дальнейшей обработке образуется бензол. Например, нагревание гидроксида натрия и хлорбензола позволяет получить натрия фенолят, который при воздействии кислоты распадается на соль, воду и фенол. Формула такой реакции приведена здесь:
С 6 Н 5 -CI + 2NaOH -> С 6 Н 5 -ONa + NaCl + Н 2 O
Ароматические сульфокислоты также являются источником для получения бензола. Химическая реакция проводится при одновременном плавлении щелочи и сульфокислоты. Как видно из реакции, сначала образуются феноксиды. При обработке сильными кислотами они восстанавливаются до многоатомных фенолов.
Фенол в промышленности
В теории, получение фенола самым простым и многообещающим способом выглядит таким образом: при помощи катализатора бензол окисляют кислородом. Но до сих пор катализатор для этой реакции так и не был подобран. Поэтому в настоящее время в промышленности используются другие методы.
Непрерывный промышленный способ получения фенола состоит во взаимодействии хлорбензола и 7% раствора едкого натра. Полученную смесь пропускают через полуторакилометровую систему труб, нагретых до температуры в 300 С. Под воздействием температуры и поддерживаемого высокого давления исходные вещества вступают в реакцию, в результате которой получат 2,4-динитрофенол и другие продукты.

Не так давно был разработан промышленный способ получения фенолсодержащих веществ кумольным методом. Этот процесс состоит из двух этапов. Сначала из бензола получают изопропилбензол (кумол). Для этого бензол алкируют с помощью пропилена. Реакция выглядит следующим образом:

После этого кумол окисляют кислородом. На выходе второй реакции получают фенол и другой важный продукт — ацетон.
Получение фенола в промышленных масштабах возможно из толуола. Для этого толуол окисляется на кислороде, содержащемся в воздухе. Реакция протекает в присутствии катализатора.
Примеры фенолов
Ближайшие гомологи фенолов называются крезолами.

Существуют три разновидности крезолов. Мета-крезол при нормальных условиях представляет собой жидкость, пара-крезол и орто-крезол - твердые вещества. Все крезолы плохо растворяются в воде, а по своим химическим свойствами они почти аналогичны фенолу. В естественном виде крезолы содержатся в каменноугольной смоле, в промышленности их применяют при производстве красителей, некоторых видов пластмасс.
Примерами двухатомных фенолов могут служить пара-, орто- и мета-гидробензолы. Все они представляют собой твердые вещества, легко растворимые в воде.
Единственный представитель трехатомного фенола - пирогаллол (1,2,3-тригидроксибензол). Его формула представлена ниже.

Пирогаллол является довольно сильным восстановителем. Он легко окисляется, поэтому его используют для получения очищенных от кислорода газов. Это вещество хорошо известно фотографам, его используют как проявитель.
По числу гидроксильных групп:
Одноатомные; например:
Двухатомные; например:

Трехатомные; например:

Существуют фенолы и большей атомности.
Простейшие одноатомные фенолы
С 6 Н 5 ОН - фенол (гидроксибензол), тривиальное название - карболовая кислота.

Простейшие двухатомные фенолы

Электронное строение молекулы фенола. Взаимное влияние атомов в молекуле
Гидроксильная группа -ОН (как и алкильные радикалы) является заместителем 1 рода, т. е. электронодонором. Это обусловлено тем, что одна из неподеленных электронных пар гидроксильного атома кислорода вступает в р, π-сопряжение с π-системой бензольного ядра.

Результатом этого является:
Повышение электронной плотности на атомах углерода в орто- и пара- положениях бензольного ядра, что облегчает замещение атомов водорода в этих положениях;
Увеличение полярности связи О-Н, приводящее к усилению кислотных свойств фенолов по сравнению со спиртами.
В отличие от спиртов, фенолы частично диссоциируют в водных растворах на ионы:

т. е. проявляют слабокислотные свойства.
Физические свойства
Простейшие фенолы при обычных условиях представляют собой низкоплавкие бесцветные кристаллические вещества с характерным запахом. Фенолы малорастворимы в воде, но хорошо растворяются в органических растворителях. Являются токсичными веществами, вызывают ожоги кожи.
Химические свойства
I. Реакции с участием гидроксильной группы (кислотные свойства)

(реакция нейтрализации, отличие от спиртов)

Фенол - очень слабая кислота, поэтому феноляты разлагаются не только сильными кислотами, но даже такой слабой кислотой, как угольная:

II. Реакции с участием гидроксильной группы (образование сложных и простых эфиров)
Как и спирты, фенолы могут образовывать простые и сложные эфиры.
Сложные эфиры образуются при взаимодействии фенола с ангидридами или хпорангидридами карбоновых кислот (прямая этерификация карбоновыми кислотами протекает труднее):

Простые эфиры (алкилариловые) образуются при взаимодействии фенолятов с алкилгалогенидами:

III. Реакции замещения с участием бензольного ядра

Образование белого осадка трибромфенола иногда рассматривается как качественная реакция на фенол.

IV. Реакции присоединения (гидрирование)

V. Качественная реакция с хлоридом железа (III)
Одноатомные фенолы + FeCl 3 (р-р) → Сине-фиолетовая окраска, исчезающая при подкислении.